3-1-4-1 化学変化とイオンまとめ
問題 1
イオン式 SO₄²⁻ の名称をなんといいますか?
正解 :硫酸イオン
問題 2
イオン式 S²⁻ の名称をなんといいますか?
正解 :硫化物イオン
問題 3
塩化物イオンを表したイオン式を選びましょう。
正解 :Cl⁻
問題 4以下の図はヘリウム原子の構造を表している。
以下の図はヘリウム原子の構造を表している。
(イ)が示すものはなんでしょうか?
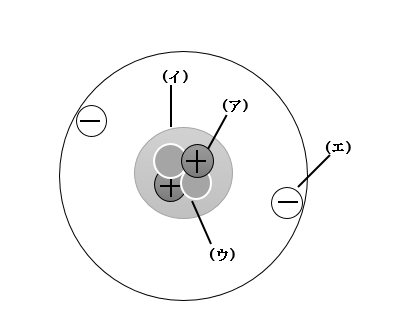
正解 :原子核
問題 5原子全体は電気を帯びていない理由として
原子全体は電気を帯びていない理由として
正しいものを選びましょう。
正解 :陽子と電子の数が等しいから
問題 6塩化ナトリウムの電離は以下のように表すことができる。
塩化ナトリウムの電離は以下のように表すことができる。
NaCl → Na⁺ + Cl⁻
塩酸の電離はどのように表せますか?
Na⁺はNa+、Cl⁻はCl-と表すこととし、空欄に+かーをいれましょう。
正解 :+,-
問題 7以下のような装置で塩化銅水溶液の電気分解を行った。
以下のような装置で塩化銅水溶液の電気分解を行った。
塩化銅水溶液の電気分解をしたときに、
銅が付着するのはどちらの極ですか?
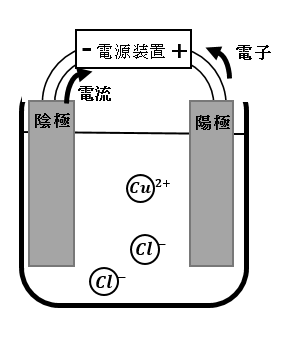
正解 :陰極
問題 8以下の図のように塩酸の電気分解を行うと、
以下の図のように塩酸の電気分解を行うと、
水素を発生させるのは
陽極と陰極の どちらですか?
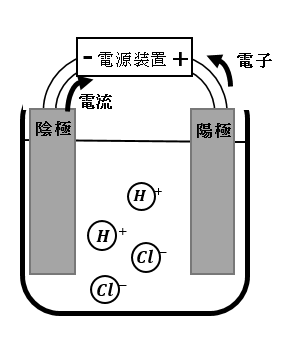
正解 :陰極
問題 9塩酸の電気分解を表す式を
塩酸の電気分解を表す式を
数字や元素記号をいれて 完成させましょう。
ただし、H₂などはH2と表すこと。
正解 :2,Cl2
問題 10以下の図のようにうすい塩酸の中に、
以下の図のようにうすい塩酸の中に、
亜鉛板と銅板をいれて電池を作った。
+極は亜鉛板と銅板のどちらですか?
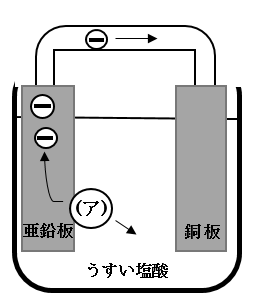
正解 :銅板
問題 11以下の図のようにうすい塩酸の中に、
以下の図のようにうすい塩酸の中に、
亜鉛板と銅板をいれて電池を作った。
しばらくするとどちらかの板が溶けて小さくなっていた。
亜鉛板と銅板どちらが溶けていきましたか?
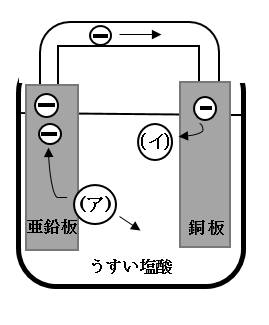
正解 :亜鉛板
問題 12以下の図のようにうすい塩酸の中に、
以下の図のようにうすい塩酸の中に、
亜鉛板と銅板をいれて電池を作った。
しばらくすると銅板に小さな泡がたくさんついていた。
これは気体が発生したということである。
この発生した気体はなんですか?

正解 :水素
問題 13水溶液においての「中性」という言葉の定義として
水溶液においての「中性」という言葉の定義として
正しいものを選びましょう。
正解 :水素イオンと水酸化物イオンが存在しない
問題 14ある液体を赤色のリトマス紙にかけると色が変化しませんでした。
ある液体を赤色のリトマス紙にかけると色が変化しませんでした。
この水溶液は何性ですか?考えられるものをすべて選びましょう。
正解 :酸性,中性
問題 15
以下の組み合わせで中和が起こるものを選びましょう。
正解 :水酸化ナトリウムと硫酸
問題 16塩酸に水酸化ナトリウム水溶液を少しずつ加えていきました。
塩酸に水酸化ナトリウム水溶液を少しずつ加えていきました。
そこにBTB溶液を入れると水溶液全体は緑色になりました。
このとき水溶液中はどちらのイオンのほうが多く含まれていますか?
正解 :どちらのイオンも同量
問題 17塩酸に水酸化ナトリウム水溶液を少しずつ加えていくと塩ができました。
塩酸に水酸化ナトリウム水溶液を少しずつ加えていくと塩ができました。
塩の名前を答えましょう。
正解 :塩化ナトリウム,食塩